| 标识符 | CSTR:16397.09.0H01001229 |
|---|---|
| 资源中文名称 | APPPS1转基因阿尔兹海默病小鼠模型 |
| 资源英文名称 | |
| 疾病概述 | 阿尔兹海默病(Alzheimer’s disease, AD) 临床症状主要为记忆障碍、失语、失用、失认、视空间技能损害、执行功能障碍以及人格和行为改变等全面性痴呆表现,起病隐匿,呈进行性发展。 病理表现主要为脑组织萎缩、神经纤维缠结、老年斑形成和大量淀粉样蛋白沉积。 发病机制尚不明确,从目前研究来看,该病的可能因素和假说多达30余种,主要发病机制假说包括Aβ毒性假说,Tau蛋白代谢异常,神经炎症,胆碱能损伤,金属离子代谢紊乱,糖脂代谢紊乱,自由基损伤,神经血管功能失调,线粒体功能紊乱,兴奋性氨基酸毒性、病毒感染等。 |
| 实验动物背景信息 | APP基因位于染色体21q11.2-22.2上,由18个外显子和17个内含子组成。基因产物为跨膜糖蛋白,由APP基因通过选择性剪切翻译而成。APP至少有六种剪接形式,长度分别为365、563、695、714、751、770个氨基酸残基,其中695、751和770为主要形式。APP695主要在大脑表达,尤其在AD病人的海马回和皮层中APP695与APP751的比率异常,且与脑中这些部位斑块的数量呈正相关。由APP编码的APP蛋白经过加工水解可产生β淀粉样蛋白(β amyloid, Aβ)。病理情况下,APP经过β分泌酶和γ分泌酶分解生成Aβ40和Aβ42,其中Aβ42与AD患者脑中Aβ沉积和神经元的变性密切相关。在家族性AD患者中已鉴定出多个APP基因的突变位点。其中大部分突变位于外显子16和17的分泌酶裂解位点或APP跨膜区,如APP瑞典突变(APPswe:APP K670N和M671L)和伦敦突变(APPlon:APPV717I)。APP突变可改变APP的加工过程,导致具有神经毒性作用的Aβ42产生,引发多种病理机制,促使神经细胞凋亡或死亡,最终导致AD的发生。 PS1基因位于14号染色体,共10个外显子。PS1基因编码的PS蛋白为γ分泌酶的重要组成部分,在生成Aβ的过程中起重要作用。PS1突变是引起家族性AD的主要原因之一。PS1突变使其编码的蛋白亲水性环状结构域缺失,导致其构象改变,可影响γ-分泌酶的活性,使Aβ42生成增多。 |
| 模型制作方法 | 1、模型制作 APP/PS1双转基因小鼠模型是利用PrP-hAPPK595N/M596L单转基因痴呆模型小鼠和PrP-hPS1dE9单转基因痴呆症模型小鼠杂交培育而成。
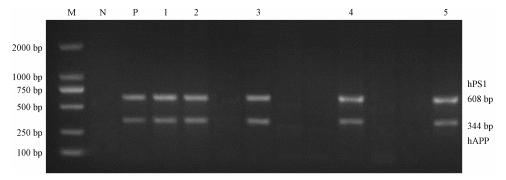
2、基因型鉴定 提取首建鼠后代鼠尾DNA,PCR扩增,1%琼脂糖凝胶电泳,结果如图1。
图1. PCR鉴定APP/PS1转基因小鼠的凝胶电泳分析结果。 M:marker;N:阴性对照;P:阳性对照;1,2,3,4,5号为APP/PS1转基因阳性小鼠 |
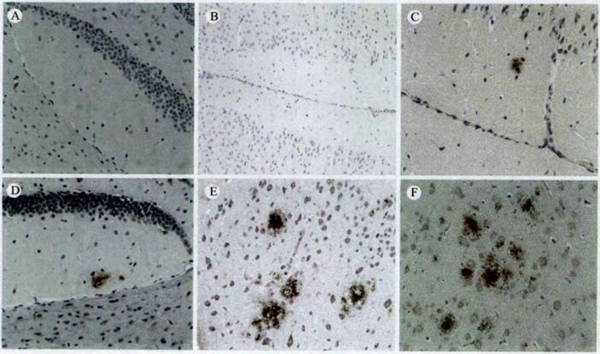
| 模型表型数据 | 3、APP/PS1转基因小鼠脑部病理表型 病理染色选用Aβ1-17抗体免疫组化(1:200),Thioflavin-S荧光染色和改良的Bieschowsky银染法均显示3月龄动物未检测到明显老年斑出现。4、5月龄时APP/PS1转基因小鼠在大脑皮层出现老年斑,随着月龄增加,大脑皮层老年斑数量体积明显增加,9-12月龄小鼠大脑出现与AD患者相似的老年斑。三种方法标记老年斑结果一致。 Aβ免疫组化染色:
图2、不同月龄APP/PS1转基因小鼠大脑Aβ免疫组化染色结果 A、3月龄APP/PS1转基因小鼠大脑海马区Aβ1-17免疫组化染色(100╳);B、4月龄APP/PS1转基因小鼠大脑皮层Aβ1-17免疫组化染色(100╳);C、4.5月龄APP/PS1转基因小鼠大脑皮层Aβ1-17免疫组化染色(200╳);D、6月龄APP/PS1转基因小鼠大脑海马区Aβ1-17免疫组化染色(100╳);E、9月龄APP/PS1转基因小鼠大脑皮层Aβ1-17免疫组化染色(200╳);F、12月龄APP/PS1转基因小鼠大脑皮层Aβ1-17免疫组化染色(200╳)
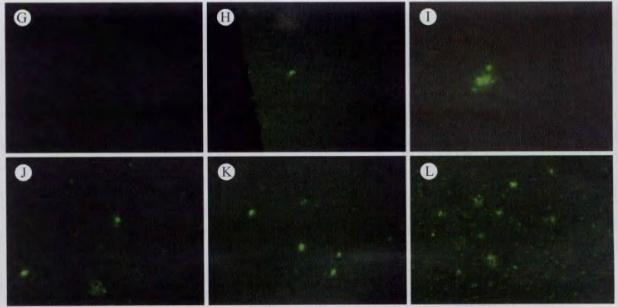
Thioflavin-S荧光染色:
图3、不同月龄APP/PS1转基因小鼠大脑Thioflavin-S荧光染色结果 G、3月龄APP/PS1转基因小鼠大脑Thioflavin-S荧光染色(200╳);H、4.5月龄APP/PS1转基因小鼠大脑皮层Thioflavin-S荧光染色(200╳);I、6月龄APP/PS1转基因小鼠大脑皮层Thioflavin-S荧光染色(200╳);J、9月龄APP/PS1转基因小鼠大脑皮层Thioflavin-S荧光染色(200╳);K、12月龄APP/PS1转基因小鼠大脑皮层Thioflavin-S荧光染色(200╳);L、AD病人大脑皮层Thioflavin-S荧光染色(200╳); 改良的Bieschowsky银染法染色
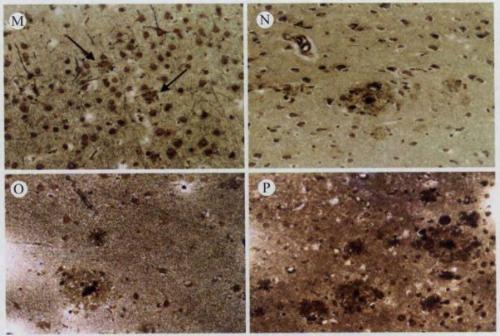
图4、不同月龄APP/PS1转基因小鼠大脑改良Bieschowsky银染法染色结果 M、4.5月龄APP/PS1转基因小鼠大脑皮层改良Bieschowsky银染法染色结果(200╳),箭头指示老年斑;N、6月龄APP/PS1转基因小鼠大脑皮层改良Bieschowsky银染法染色结果(200╳);O、9月龄APP/PS1转基因小鼠大脑皮层改良Bieschowsky银染法染色结果(200╳);P、12月龄APP/PS1转基因小鼠大脑皮层改良Bieschowsky银染法染色结果(200╳)
4、APP/PS1转基因小鼠电镜检查海马组织超微结构变化 电镜结果显示野生对照小鼠海马神经元细胞无异常,AD模型组小鼠海马组织内可见萎缩的神经元,细胞体积缩小,细胞核轮廓不清,染色质边集,核仁消失,胞浆浓缩。部分神经元变性,细胞表面呈现复杂的质膜内褶,胞浆内可见大量脂滴和脂褐素沉积,细胞核边缘皱褶,染色质均匀化。核周隙增宽,核膜局部断裂崩解,染色质边集。胞浆内线粒体病变明显,部分线粒体体积增大、变形、局部崩解、基质肿胀、嵴肿胀溶解。可见线粒体内包涵物。内质网扩张,高尔基体变形。神经纤维内微管解聚。线粒体肿胀,轮廓模糊,嵴溶解。断裂突触肿胀,突触小泡减少,突触内线粒体变形,线粒体肿胀溶解。可见大量变性的神经突,早期可见浓缩的轴浆、变性的线粒体、自噬空泡和电子密度不等的膜包颗粒。小胶质细胞内可见吞噬的淀粉样物质,部分胶质细胞固缩。
图5、APP/PS1转基因小鼠海马组织超微结构(8-9月龄)
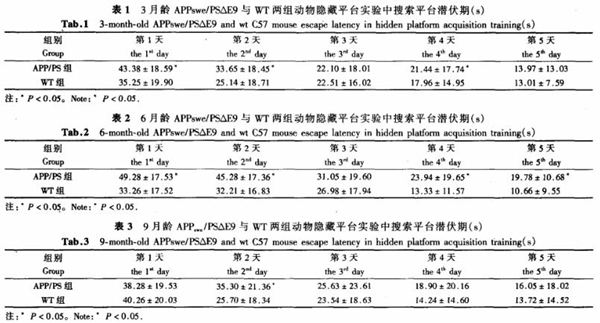
5、APP/PS1转基因小鼠行为学表现 水迷宫实验 Morris水迷宫实验发现3、6、9月龄APP/PS1转基因小鼠空间探索实验结果与同月龄野生型小鼠相比具有显著差异,学习及记忆能力显著降低(P<0.05)。
|
| 动物模型的评价与验证 | |
| 保存方式 | |
| 合作方式 | |
| 相关文章 |
1、宗园媛,王晓映,王海林,刘亚莉,黄澜,马春梅,张连峰,秦川. APP/PS双转基因阿尔茨海默病小鼠模型的老年斑及行为学动态分析[J]. 中国比较医学杂志. 2008. 18(9). 2、宋楠,张玲,陈巍,张倩,韩云林,秦川. 矢车菊素-3-葡萄糖苷对APPswe/PS1ΔE9阿尔茨海默病模型小鼠糖脂代谢的影响[J]. 中国比较医学杂志. 2016,26(7):15-23. 3、朱皓,高凯,张连峰. 阿尔兹海默病小鼠模型的磁共振影像学分析[J].中国比较医学杂志. 2012,(12):48-53. 4、史长华,张玲,陈巍,付信靖,秦川. RNA-Seq 技术筛选APP/PS1阿尔茨海默病模型小鼠差异表达基因及功能分析[J].中国比较医学杂志. 2018,28(10):1-7. 5、梁良. 中药I号方对阿尔兹海默病的多靶位治疗作用[J].中国比较医学杂志. 2013,23(5). 6、秦川,吴善球,陈保生,吴小闲,屈焜耀,刘军民,张桂芳,徐艳峰,舒顺利,孙丽华,李彦红,朱华,黃澜,马春梅,徐玉环,韩云林,卢耀增. 灵芝制剂治疗APP/PS-1阿尔茨海默病转基因小鼠模型的病理学改变[J].中国医学科学院学报. 2017年第4期. 7、Ling Zhang, Ying Wang, Xia Xiayu, Changhua Shi, Wei Chen, Nan Song, Xinjing Fu, Rui Zhou, Yan-Feng Xu, Lan Huang, Hua Zhu, Yunlin Han and Chuan Qin∗. Altered Gut Microbiota in a Mouse Model of Alzheimer’s Disease[J]. Journal of Alzheimer’s Disease 60 (2017) 1241–1257. 8、Yan Liu, Yan-Feng Xu, Ling Zhang, Lan Huang, Pin Yu, Hua Zhu, Wei Deng, Chuan Qin∗. Effective expression of Drebrin in hippocampus improves cognitive function and alleviates lesions of Alzheimer’s disease in APP (swe)/PS1 (ΔE9) mice[J]. CNS Neurosci Ther. 2017 Jul;23(7):590-604. |
| 备注 |



 京公网安备 11010502043083号
京公网安备 11010502043083号