| 标识符 | CSTR:16397.09.0C01000818 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 资源中文名称 | 盐酸诱导小鼠急性肺损伤模型 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 资源英文名称 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 疾病概述 | 急性肺损伤(acute lung injury,ALI)是由非心源性的各种严重肺内外致病因素如严重感染休克、创伤、DIC、误吸等原发疾病引起,临床主要表现为急性进行性加重的呼吸困难和难治性低氧血症,进一步发展可演变为急性呼吸窘迫综合征(ARDS)[1]。虽然ALI的病因多样,但研究显示它们是严重损伤引起机体全身免疫炎症反应失控过程中的不同阶段。而肺脏则是这一过程中最易受损的首位靶器官,所以ARDS出现最早发病率也最高。 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 实验动物背景信息 | 1.C57bL/6J小鼠 ,专业名称:C57bL/6J,近交系(Inbred Rat) 品系来源 :1921年 C.C.Little用 Lathrop小鼠作近亲培育时,用No7雄鼠和No.52雌鼠交配,培育成C57。在C57中将毛色呈黑色的进行固定,培育成C57BL。1937年Ltle将维持的C57BL第六组亚系定名为C57BL6,将第十组亚系定名为C57BL10,继而分别维持至今。1947年从 Little引入到美国 Jackson Lab,形成C57BL/6J:1951年从 Jackson Lab将第32代引入到NH,形成c57BL6N亚系;1974年 Charles River从NH引入并于1975年进行了剖腹产。六十年代从 Jackson Lab引入到日本实验动物中央研究所,1986年自日本实验动物中央研究所引入到中科院上海实验动物中心。2001年中国北京维通利华从美国 Charles River引入第59代核心群。 2.盐敏感大对照鼠SS-13BN Rat,专业名称:SS-Chr13BN/McwiCrlVr,Ø同类系(Consomic Rat) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 模型制作方法 | 诱导方法:自制气管滴注导管,动脉导管( 内径0.28mm, 427401, BD Intramedic PE Tubing),长度4cm,插入端加热制成一定弧度, 动物麻醉后颈前暴露气管,充分暴露喉部以及声门,配合冷光源的使用,可见光源由声门处透射出并随声门开合呈现闪烁感( Fig2A);于声门张开瞬间,右手持导管向前上方平稳插入气管,有轻微突破感,拔出导丝,调整导管向左侧弯曲,缓慢向气管深处插入,深至距小鼠上门牙约2.8cm以确保导管末端置于左主支气管内,末端连接胰岛素注射器,向导管内缓慢推注0.1M浓度盐酸或生理盐水对照),推注过程大于10s,再补推注入约30倍液体体积的空气。竖直放置小鼠5min,术后小鼠给予保温措施等待苏醒,密切观察至72h,存活动物为成功造模动物。 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 模型表型数据 | 1.左肺弥漫性出血、渗出,而右肺损害不明显,
Fig1 肺部大体解剖 2 肺泡灌洗液白细胞计数和蛋白浓度、肺湿干重比结果见表3~5。I ) 盐酸组与生理盐水组比较,肺泡灌洗液中白细胞计数呈显著增加;除30 min时间点, HCl组与相对应的各个时间点NS组的比较,其差异有统计学意义(P<0.05),并在6 hHCl组达到峰值(P值<0.01)。II ) 肺泡灌洗液蛋白浓度6 h NS组时BALF蛋白浓度出现轻度升高(P值<0.05 vs 12 h组);HCl刺激6 h时达峰值并明显高于6 h NS组及其它时间点HCl 组。III )左肺肺湿干重比值(W/D)在HCl刺激30 min时明显升高,12 h达峰值后呈下降趋势,至24小时进一步恢复。 Tab 3 各组BALF WBC (×10^7/L x±s)
*P值<0.01 vs相应时间点NS组; #P值<0.05 vs 2 h组; ▲P值<0.05 vs 12 h组 Tab 4 各组BALF蛋白浓度 (μg/μl x±s)
*P值<0.01 vs相应时间点NS组; #P值<0.05 vs 2 h组; ▲P值<0.05 vs 12 h组vs 24 h组 Tab 5 各组肺湿干重比 W/D (% x±s)
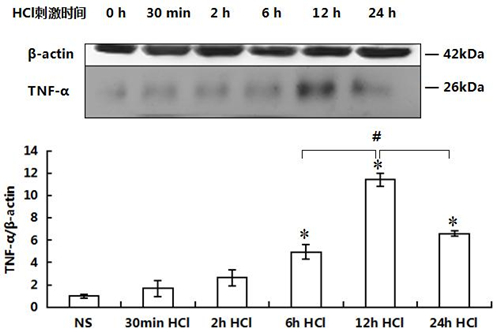
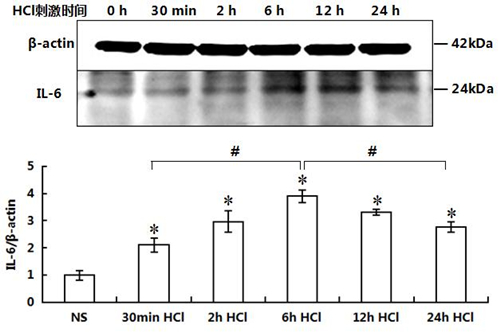
*P<0.01 vs相应时间点NS组; #P值<0.05 vs 6 h组 TNF-α、IL-6、IL-1β和NF-κB免疫印迹检测 NS组各时间点组肺组织TNF-α、IL-6、IL-1β和NF-κB的蛋白表达量无显著差异, HCl组6、12和24 h显著升高( P值<0.01 vs NS组),在12 h HCl组达到峰值( P<0.05 vs 6 h 、24 h HCl组,Fig2);肺组织IL-6蛋白表达量比较HCl组30 min开始显著升高( P<0.01 vs NS组), 6 h HCl组达到峰值( P<0.01 vs NS组,P<0.05 vs 30 min、24 h HCl组,Fig3);肺组织IL-1β 蛋白表达量比较,HCl组30 min开始显著升高( P<0.05 vs NS组),在6 h HCl组达到峰值( P<0.05 vs NS组, P<0.05 vs 2 h、24 h HCl组,Fig4);肺组织NF-κB蛋白表达量比较,HCl组30 min开始升高,在2 h、6 h和12 h HCl组表达量显著升高( P<0.05 vs NS组,Fig5)。
Fig2 小鼠肺组织TNF-α 表达水平 *P值<0.05 vs NS组, #P值<0.05
Fig3 小鼠肺组织IL-6表达水平 *P值<0.05 vs NS组, #P值<0.05
Fig4 小鼠肺组织IL-1β 表达水平 *P值<0.05 vs NS组, #P值<0.05
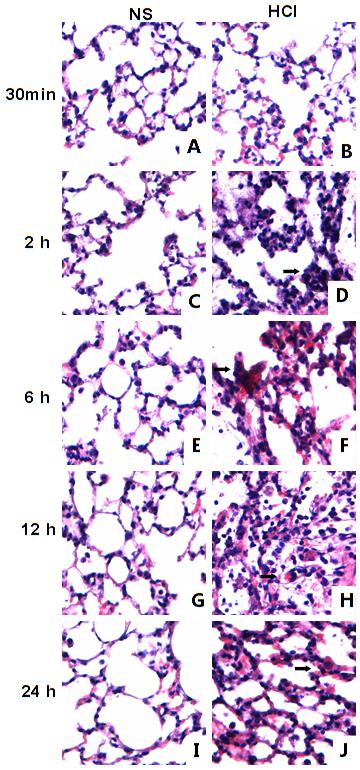
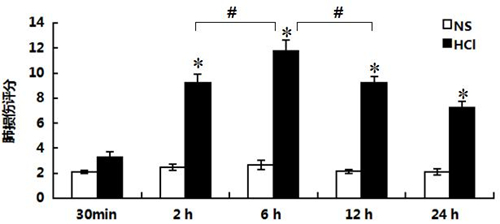
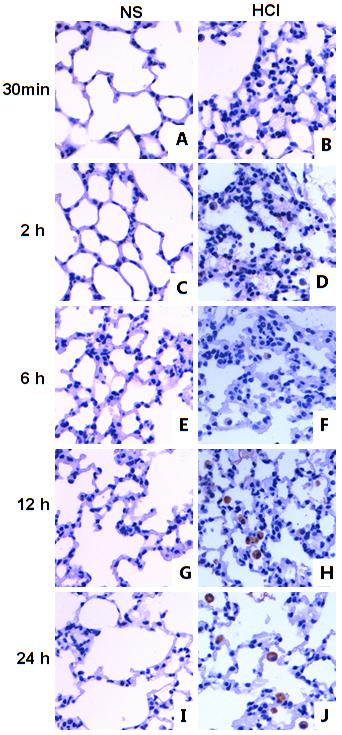
Fig5 小鼠肺组织NF-κB表达水平 *P值<0.05 vs NS组 1.病理学结果及肺损伤评分 NS组各时间点肺组织观察可见肺泡结构完整、清晰,无损害( Fig6 );30 min HCl 组的肺组织未见明显损害或轻微损害,肺泡结构较完整, 肺泡间隔无明显水肿,有少量炎性细胞浸润( Fig6B);2 h HCl组,弥漫性肺泡壁增厚、红细胞渗出和炎性细胞浸润( Fig6D黑色箭头所示);6 h HCl组,肺组织损害显著,肺组织弥漫性的出血、水肿,肺泡壁增厚、结构紊乱,部分肺泡萎陷不张( Fig6F黑色箭头所示);12 h HCl组较6 h HCl组损害程度减轻,肺间质轻中度水肿,肺泡结构破坏程度以及炎性细胞浸润较6 h组减轻( Fig6H黑色箭头所示);24 h HCl组,肺组织水肿充血程度仍然较重,与6、12 h组相比肺部炎症程度较轻( Fig6J黑色箭头所示)。HCl 组与NS组各个时间刺激点相比较, (除外30 min) 的肺组织病理损伤评分显著升高,且差异有统计学意义(P<0.001);并且HCl组,6 h HCl 组肺损伤评分与2 h、12 h HCl组比较显著升高,且差异有统计学意义(P值<0.05)。
Fig6 小鼠肺病理学改变 (H&E染色 ×400)
Fig7 肺损伤评分 与NS组比较显著升高 *P值<0.001;6h组与2 h、12 h HCl组比较显著升高 #P值<0.05; 2. 肺组织免疫组化结果 CD3为T淋巴细胞膜表面标记物,12 h HCl 组可见肺间质出现T淋巴细胞(CD3+)(Fig8H),24 h时仍大量存在( Fig8J);以CD68为细胞膜表面标记物的巨噬细胞,在6 h HCl 组的肺间质出现( Fig9F),至24 h时仍然大量存在( Fig9J);Gr-1主要为粒细胞膜表面标记物,30 min HCl 组开始在肺泡间质出现,部分与肺泡壁黏附,至24 h时仍然大量存在(Fig10)。
Fig8 肺组织CD3免疫组化-T淋巴细胞 (×400)
Fig9 肺组织CD68免疫组化-巨噬细胞 (×400)
Fig10 肺组织Gr-1免疫组化-嗜中性粒细胞 (×400) 呼吸功能(Pehn): HCl刺激小鼠6-12 h时出现Pehn明显升高,提示起到阻力显著增加 Tab 6 各组呼吸功能 Pehn (x±s)
*P值<0.01 vs相应时间点NS组; #P值<0.05 vs 2 h组; ▲P值<0.05 vs 24 h组 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 动物模型的评价与验证 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 保存方式 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 合作方式 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 相关文章 |
[I] Atabai K, Matt hay MA. The pulmonary physician in critical care. 5:acute lung injury and the acute respiratory dist resssyndrome definitions and epidemi dlog. Thorax2002.57:452-458 [2]毛宝龄钱桂生陈正堂急性肺损伤和急性呼吸窘迫综合征M第1版 北京人民卫生出社20021-6 [3]孙海鹏,呼彩莲,急性肺损伤发病机制的研究J.医学信息2010年02月第23卷第二期,532—533 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 备注 |







 京公网安备 11010502043083号
京公网安备 11010502043083号