| 标识符 | CSTR:16397.09.0L01001207 |
|---|---|
| 资源中文名称 | 双侧外耳缺失伴发外耳道闭锁的猪动物模型 |
| 资源英文名称 | |
| 疾病概述 | 小耳畸形的病因目前还不完全明确,环境和遗传因素是目前小耳畸形病因研究的重点。小耳畸形主要涉及胚胎发育期间第一和第二鳃弓的异常,主要表型涉及外耳发育异常。外耳的耳廓是由第一和第二鳃弓的逐渐融合形成的,在发育过程中第一和第二鳃弓之间是相互作用,两弓之间的凹槽加深,形成外耳道。 |
| 实验动物背景信息 | 以二花脸公猪和沙子岭母猪为祖代个体,构建近交群体。HOXA1基因突变筛查: 由于HOXA1基因编码区的c.451G>TC突变导致 |
| 模型制作方法 | 二花脸×沙子岭F2近交群体:此群体由1头二花脸公猪和1头沙子岭母猪杂交,选取全同胞的1头F1公猪和1头F1母猪,互交六胎次,生产F2个体。 |
| 模型表型数据 | 二花脸×沙子岭F2近交群体,患病个体为双侧外耳缺失伴发外耳道闭锁,颞部CT显示为双侧外耳道闭锁、中耳结构发育不良;进一步的基因检测为HOXA1纯合突变。HOXA1基因纯合突变的猪动物模型,复合人类双侧小耳畸形畸形特征,为其进一步在小耳畸形病理机制中的应用提供基础。
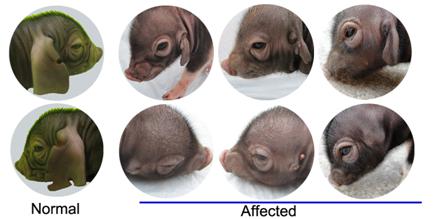
1. 动物模型查体 与正常个体相比,患病个体表现为:外耳明显变小甚至完全缺失,见于双侧耳;外耳道完全闭锁、少数仅仅存留一个瘘管样结构;身材矮小;呼吸急促;几乎不主动吃奶,人工喂养时也不能正常进食;呆滞;平衡感差;出生后两周内死亡。
图 1 全同胞患病和正常仔猪的外耳表型图
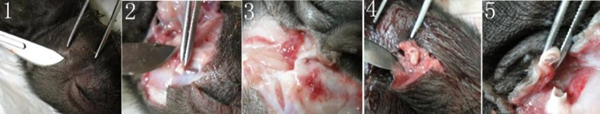
为了进一步了解患病仔猪的各器官组织的发育情况,我们选择了3头患病个体进行解剖观察。结果显示患病个体的各器官组织无明显发育异常。沿着外耳道闭锁的小孔剪开患病个体的面部表皮和肌肉组织后,可见外耳道缺失;呈现为瘘管样小孔向里延伸形成发育不良的狭窄外耳道,底部闭锁未见鼓膜。
图 2 患病仔猪耳部解剖图 注:患病个体的外耳闭锁为一个小孔,如1所示。剪开皮肤组织,可见有些患病个体具有狭窄的外耳道,如2和3所示;有些患病个体的外耳道呈游离状态,如4所示。5为正常的外耳道。 2. CT检测 为了明确患病个体的中耳及内耳情况,我们选择了1头正常个体和它的1头全同胞双侧耳朵缺失的患病个体,进行128层螺旋CT(Definition AS128,西门子,德国)头部扫描。扫描结果显示:患病个体双侧外耳道闭锁消失。中耳发育畸形。内耳未见明显异常。
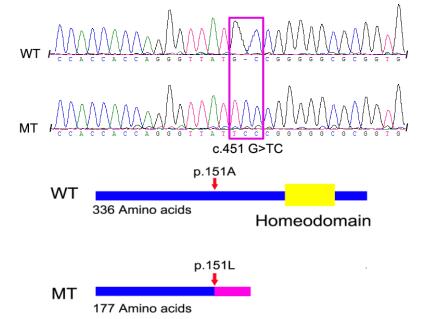
图 3 全同胞正常和患病个体的头部螺旋CT 注: 左侧为正常个体,具有正常的外耳道(EAM)和乳突(MP), 图中的标尺线为5mm;右侧为患病个体,无外耳道(EAM)和乳突(MP),图中的标尺线为5mm。 3. HOXA1基因突变检测 突变位于HOXA1基因CDS区的第451个碱基处,由G突变为TC,即c.451G>TC,患病个体和两头F0个体的sanger测序峰图如图所示。ORF分析表明此缺失插入突变造成了HOXA1蛋白翻译移框,导致第151位的丙氨酸A突变为亮氨酸L,从第151位氨基酸开始往后的所有氨基酸序列都发生改变,还形成了一个新的终止密码子TAA,使HOXA1蛋白的翻译提前终止,编码的氨基酸由336个减少为177个。功能分析表明突变蛋白缺少了HOX基因家族唯一的功能结构域homeobox。
图4 c.451G>TC的测序峰图及突变蛋白示意图 |
| 动物模型的评价与验证 | |
| 保存方式 | |
| 合作方式 | |
| 相关文章 | 双侧外耳缺失伴发外耳道闭锁的猪动物模型鉴定及其在整形外科的应用.中华整形外科杂志, 2018,34(3):232-236. |
| 备注 |



 京公网安备 11010502043083号
京公网安备 11010502043083号