| 标识符 | CSTR:16397.09.0H16001164 |
|---|---|
| 资源中文名称 | 帕金森疾病恒河猴基因修饰模型 |
| 资源英文名称 | |
| 疾病概述 | 帕金森病(Parkinson′s disease,PD)是一种常见的神经系统变性疾病,老年人多见,平均发病年龄为60岁左右,40岁以下起病的青年帕金森病较少见。我国65岁以上人群PD的患病率大约是1.7%。大部分帕金森病患者为散发病例,仅有不到10%的患者有家族史。帕金森病最主要的病理改变是中脑黑质多巴胺(dopamine, DA)能神经元的变性死亡,由此而引起纹状体DA含量显著性减少而致病。导致这一病理改变的确切病因目前仍不清楚,遗传因素、环境因素、年龄老化、氧化应激等均可能参与PD多巴胺能神经元的变性死亡过程。 |
| 实验动物背景信息 | 在人类,PINK1突变导致常染色体隐性遗传和早发性帕金森病(PD)并伴有选择性神经变性。虽然已经在小鼠及猪产生了相关的疾病模型,但是这些模型并不能概括在PD患者中看到相关的神经变性,这意味着PINK1在哺乳动物大脑中的功能需要使用更接近人类的较大动物进行评估。 PINK1基因缺失恒河猴存在神经变性的表现,且观察到的显著神经元丢失,揭示了PINK1在灵长类大脑中的关键功能,并将提供一个新的研究PINK1的多种功能和与PINK1功能障碍相关的发病机制的工具。
|
| 模型制作方法 | 该模型使用CRISPR / Cas9介导方法引入恒河猴胚胎,然后通过辅助生殖方式植入受体动物,生产出基因修饰恒河猴,并进行动物表型评价。 |
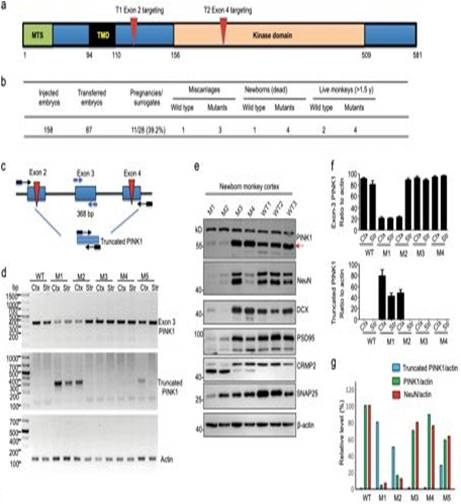
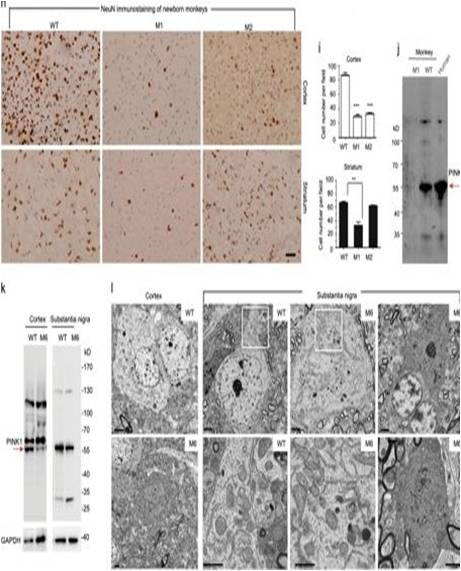
| 模型表型数据 | 在实验动物存活的猴中,8个携带PINK1突变(M),3个是野生型(WT)。然而,三只突变猴(M1,M3和M4)是新生三胞胎,它们在出生后3-4天内难以存活并死亡。一只WT新生猴也死亡。另一只突变猴(M2)在出生后7天死亡,没有明显的症状。其他三只突变猴(M6,M7和M8)已经存活了三年;然而,M5减少了食物摄入并在1.5年时显示出虚弱状态,并且在麻醉后30天死于MRI检查。
对于存活时间较短的猴,研究人员发现在M1皮质和纹状体以及M2皮质中约65%-70%的PINK1等位基因携带~7.2kb缺失。 PINK1突变猴脑的蛋白质印迹分析也证实了PINK1,神经元蛋白(NeuN,PSD95,CRMP2和SNAP25)和双皮质素(DCX)的不同程度的缺陷。对于活猴,MRI和视频监测研究显示,具有PINK1突变的1.5岁成年猴显示皮质中的灰质密度显著降低。尽管睡眠行为没有改变,M5和M6猴子也表现出运动减少。 对M6猴脑基因组DNA的分析也显示PINK1外显子2和外显子4在各种组织中的大量缺失,并且蛋白质印迹分析显示皮质和黑质中PINK1表达与年龄相比显著降低。
通过对该模型的研究,能更好地了解帕金森病的病因,发病机制,病理特征以及预防和治疗。 |
| 动物模型的评价与验证 | |
| 保存方式 | 活体保种 |
| 合作方式 | |
| 相关文章 | CRISPR/Cas9-mediated PINK1 deletion leads to neurodegeneration in rhesus monkeys. |
| 备注 |



 京公网安备 11010502043083号
京公网安备 11010502043083号