| 标识符 | CSTR:16397.09.0F01001464 |
|---|---|
| 资源中文名称 | 人体非酒精性脂肪肝肠道菌群移植小鼠模型 |
| 资源英文名称 | Human nonalcoholic fatty liver intestinal microbiota transplantation mouse model |
| 疾病概述 | 非酒精性脂肪性肝病(NAFLD)是代谢综合征在肝脏的表现形式,与肥胖 、胰岛素抵抗(IR) 、空腹高血糖症、血脂异常、脂肪因子变异等机体代谢异常明显相关,是目前慢性肝病最常见的病因。NAFLD是以过量的脂质在肝细胞内堆积为特征的连续疾病谱,可由单纯的肝脂肪性变性发展为非酒精性脂肪性肝炎(NASH),严重时可发展为肝纤维化和肝硬化 ,NASH一旦合并肝纤维化或肝硬化则可进一步增加肝细胞癌(HCC)的发生风险。 到目前为止,NAFLD的确切发病机制尚不清楚,也缺乏特异性的治疗措施,因此针对发病机制和潜在治疗药物的研究是目前该领域的热点。动物模型可通过模拟不同的病因以及NAFLD每个阶段的组织病理学和病理生理学改变,为了解NAFLD发病机制和进展提供关键性的指导。 |
| 实验动物背景信息 | C57BL/6小鼠 |
| 模型制作方法 | 实验材料 1.1实验动物 选择无特定病原体(SPF)级C57BL/6J小鼠,8-10周龄,体质量20-25g,按体重随机分组,对照组14只,非酒精性脂肪肝组11只,5只/盒饲养于SPF级屏障系统中,温度( 22±2) ℃,湿度50%~60%,12 h 循环照明,小鼠自由摄取食、水。 1.2人类粪便样本 受试者拟参与样本采集和信息采集一次,排除消化系统其它器质性疾病、消化道进行过手术者,排除有酗酒史、糖尿病、癌症、肾衰、中风等其它影响肠道菌群的疾病者,排除取样前4周服用益生菌、抗生素、非甾体类药物者。 将BMI值在18.5-23.9 kg/m2范围内,生化指标正常的健康志愿者,作为对照组;将非酒精性脂肪肝患者作为非酒精性脂肪肝组。采集受试者新鲜粪便,按照使用说明书用粪便微生物基因组保护液套装采集后存储于-80℃,离心取上清液作为粪便移植液。 2.实验方法 2.1动物模型制备 将健康对照组和非酒精性脂肪肝组人类粪便移植液,以400ul/天,连续三天经口灌胃,接种无菌小鼠,得到菌群移植小鼠。移植周期为10周,饲养在隔离环境内。 2.2标本采集及处理 实验期间每周称量小鼠体重,每周记录进食量、进水量,每2周取粪便进行16SRNA测定。实验结束后,对照组和非酒精性脂肪肝组小鼠脱毛照B超。三溴乙醇腹腔注射麻醉,腹主静脉采血至死亡。全血EDTA抗凝,室温静置30 min后,3,000 rpm,4°C离心15 min分离血清,-80℃冰箱冻存。 解剖小鼠腹腔,PBS心脏灌流,取心、肝、脾、肺、肾,滤纸吸干后称重、拍照。脾脏进行免疫学检测,心、肝、肺、肾部分组织福尔马林固定,后续石蜡包埋进行HE染色;剩余部分提取蛋白和RNA,-80℃冰箱冻存进行后续检测。部分肝脏组织冰冻切片包埋剂包埋并切片,进行病理染色。 |
| 模型表型数据 | 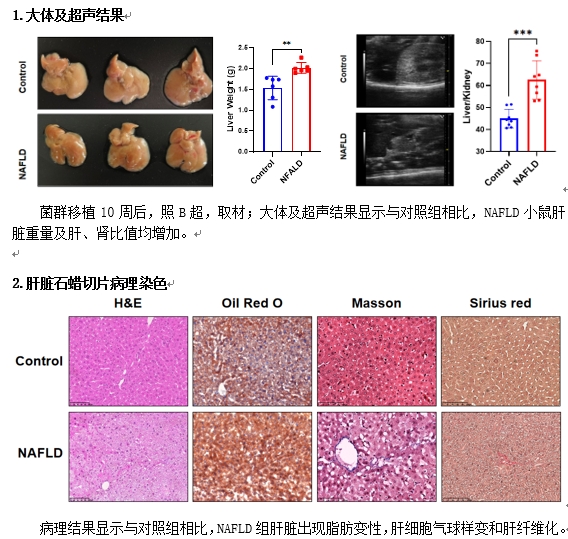 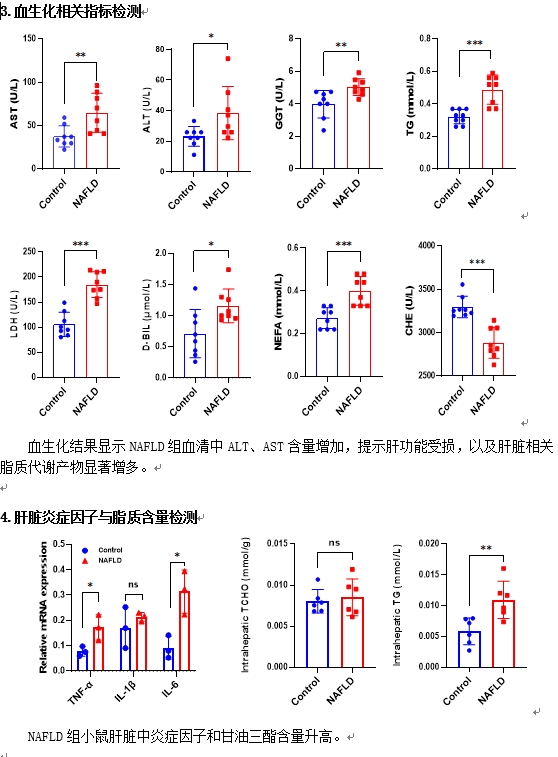 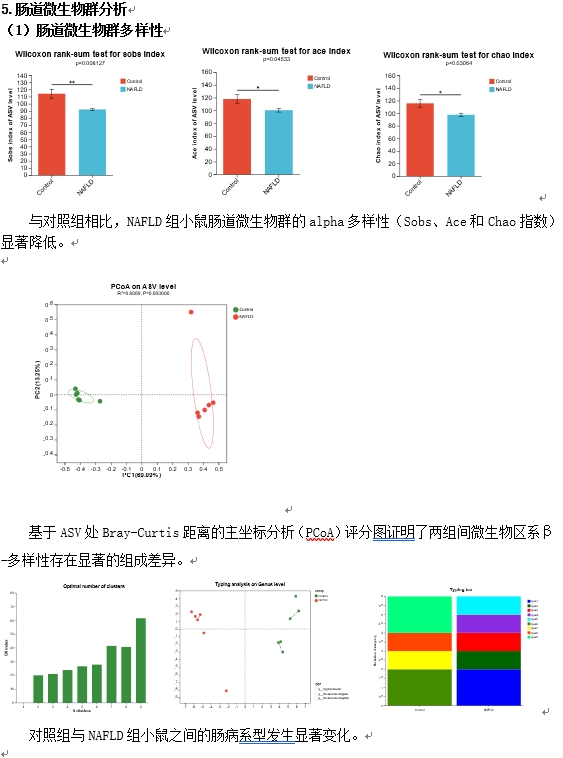  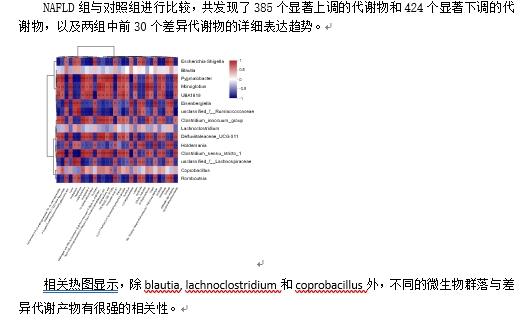 |
| 动物模型的评价与验证 | |
| 保存方式 | 冷冻 |
| 合作方式 | 不限定 |
| 相关文章 |
[1] Flessa CM, Nasiri-Ansari N, Kyrou I, Leca BM, Lianou M, Chatzigeorgiou A,Kaltsas G, Kassi E, Randeva HS. Genetic and Diet-Induced Animal Models for Non-Alcoholic Fatty Liver Disease (NAFLD) Research. Int J Mol Sci. 2022 Dec 13;23(24):15791. [2] Denk, H.; Abuja, P.M.; Zatloukal, K. Animal models of NAFLD from the pathologist’s point of view. Biochim. Biophys. Acta Mol.Basis Dis. 2019, 1865, 929–942. [3] Santhekadur, P.K.; Kumar, D.P.; Sanyal, A.J. Preclinical models of non-alcoholic fatty liver disease. J. Hepatol. 2018, 68, 230–237. |
| 备注 |


 京公网安备 11010502043083号
京公网安备 11010502043083号